Сабақ тақырыбы: Атом құрылысы. Энергетикалық деңгейлердің және олардың сыйымдылығы. Период. Топтар.
Оқу мақсаттары: Атом құрылысымен танысу және химиялық элементтердің протон, нейтрон, электрон сандарын анықтап үйрену
Анықтама. Заттың химиялық бөлінбейтін ең ұсақ бөлшегі атом деп аталады.
1911 жылы ағылшын ғалымы Эрнест Резерфорд атомның ұүрамында оң зарядты бөлшектер бар екендігін (ядро) тәжірибе жолымен дәлелдеді және атом құрылысының планетарлық моделін ұсынды.
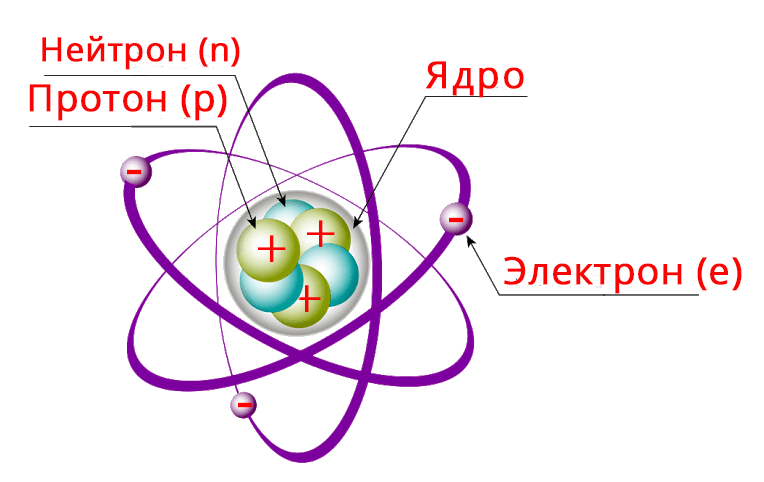
1-сурет. Атом құрылысының планетарлық моделі.
Атом ядро мен оның айналасында үнемі қозғалыста болатын электрондардан құралады. Атом ядросы протон мен нейтрон деген бөлшектерден құралады.
1-кесте. Протон, нейтрон және электрон бөлшектері жайлы мәліметтер
|
Бөлшек |
Заряды |
Таңбалануы |
Негізгі салмағы |
м.а.б. * |
|
Протон |
+(p+) |
11p |
1,673 * 10-24 г |
1 |
|
Нейтрон |
0 (n0) |
01n |
1,675 * 10-24 г |
1 |
|
Электрон |
- (e-) |
-10e |
9.109 * 10-28 г |
0 |
*м.а.б. - массаның атомдың бірлігі, бөлшектердің протон массасына қатынасы.
Анықтама: Атомдардың белгілі бір түрін химиялық элемент деп атаймыз.
Айналадығы заттардың барлығы белгілі бір химялық элементтерден құралған. Химиялық элементтердің периодтық жүйесінде қазіргі таңда белгілі 118 химиялық элементтер жеке таңбаларымен белгіленген. Әр химиялық элементтің өзіне тән қайталанбас құрылымы бар. Атом құрамындағы бөлшектер санын анықтау төмендегі формула арқылы есептеледі:
N = Ar - Z (1)
Мұндағы: N - химиялық элемент құрамындағы нейтрон бөлшектерінің саны; Ar - химиялық элементтің атомдық массасы (периодтық жүйеден алынады); Z - химиялық элементтің периодтық жүйедегі реттік нөмірі.
Химиялық элементің құрамындағы протондар саны мен электрондар саны бір-біріне тең (атом электрбейтарап бөлшек) және олардың саны химиялық элементтің периодтық жүйедегі реттік нөміріне ( Z) тең болады.
Яғни, химиялық элементтің құрамындағы бөлшектер саны әрбір элемент үшін жеке есептеледі.
Мысалы, сутегі атомы (Н) құрамындағы бөлшектер санын есептейік.
Шешуі: 1) Химиялық элементтердің периодтық жүйесінен (ХЭПЖ) сутегі атомының салыстырмалы атомдық массасы мен реттік нөмірін жазып алайық.
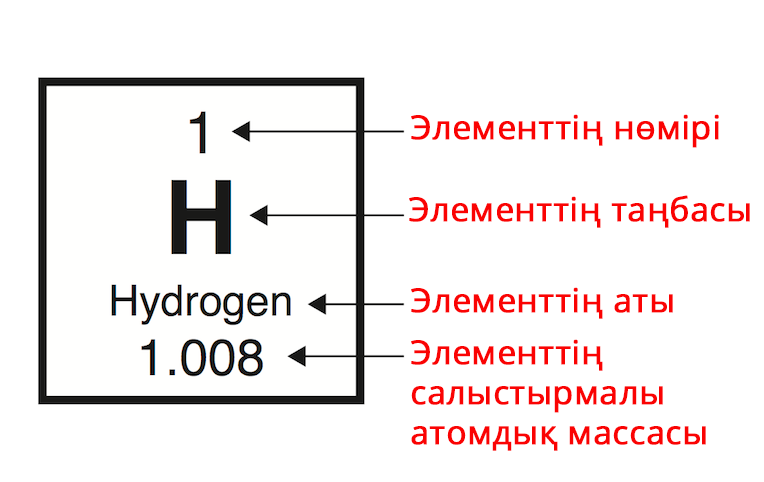
2-сурет. Сутегі химиялық элементінің периодтық кестеде белгілнеуі.
Сонда, Сутегі атомы үшін:
Ar = 1 м.а.б. ; Z= 1.
N=Ar- Z=1-1=0.
Сутегі атомында бір протон, бір электрон бар, нейтрон бөлшектері - жоқ екендігін табамыз. Атом құрылысын келесі жолмен өрнектейміз:
11Н(1р+; 0n-)1e-
Күн жүйесінде әр планета өз орбитасымен ғана қозғалатындығын және әр орбита - бір планета жолы екендігін білеміз. Ал химиялық элемент атомдарында электрондар - энергетикалық деңгейлер бойымен қазғалады және әр энергетикалық деңгейдің сыйымдылығы әр түрлі болады.
Анықтама: Химиялық элементтердің периодтық жүйесіндегі көлденең жолақтарды периодтар, ал тігінен тұрған бағандарды топтар деп атаймыз.
Энергетикалық деңгейлер санын- период нөмірі анықтайды. Бір периодта орналасқан элементтердіц знергетикалық деңгейлер саны бірдей болады.
Мысалы: азот (N) және оттегі (О) элементтерінің электрондары қанша деңгейде орналасатындығын анықтайық.
Шешуі: азот (N) және оттегі (О) элементтері - екінші периодта орналасқан. Азот элементінің реттік нөмірі: Z = 7; Оттегі элементінің реттік нөмірі: Z = 8. Яғни, азот атомының 7 электроны және оттегі элементінің 8 электроны екі энергетикалық деңгейге орналасады.
2-кесте. Энергетикалық деңгейлерде максималды электрондар саны
|
Энергетикалық деңгей нөмірі |
Электрондардың максималды саны N (N=2n2 , n- период нөмірі) |
|
1 (K) |
2 |
|
2 (L) |
8 |
|
3 (M) және т.б. |
18 |




