Сабақ тақырыбы: Электролиттер мен бейэлектролиттер. Электролиттік диссоциациялану теориясы.
Оқу мақсаттары:
Электролиттер мен бейэлектролиттердің анықтамасын білу;
Электролиттік диссоциация теориясын білу;
Электролиттік диссоциация механизмін білу;
Анықтама.
Ертіндіде және балқымасында тоқ өткізетін заттар – электролиттер деп аталады.
Ертіндісінде және балқымасында тоқ өткізбейтін заттар – бейэлектролиттер деп аталады
Электролиттің ионға ыдырау процесі электролиттік диссоциация деп аталады (ЭД)
Заттар электр өткізгіштігіне қарай электролиттер және бейэлетролиттер деп жіктелінеді. Электролиттер мен бейэлектролиттер сулы ерітіндісі немесе балқыма күйінде бола алады. Ертіндіде заттар суда ерітіледі, ал балқымада сусыз тек заттарды жоғары температурада балқыған күйін айтады.
Электролиттер мен бейэлектролиттер бір-бірімен химиялық байланыс түріменде ерекшелінеді:
Электролиттер - ионды және ковалентті полюсті байланысы бар заттар. Олар еритін қышқылдар, негіздер(сілтілер) және тұздар. Мысал ретінде: НСl, KOH, NaCl т.с.с заттарды айтуға болады.
Бейэлектролиттер - Ковалентті полюссіз және әлсіз полюсті байланысы бар заттар. Олар жай заттар, оксидтер және ерімейтін қышқылдар, негіздер мен тұздар және органикалық заттардың көпшілігі. Мысал ретінде: О2 , H2SiO3, Zn(OH)2, CaCO3, спирттер, көмірсулар және т.б.
Зертханада электролиттер мен бейэлектролиттерді қалай ажырата аламыз?
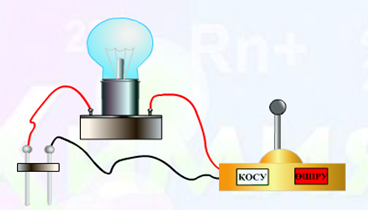
Сурет 1
1-суретте екі электр өткізгіш қабілеті бар электродтар. Электродтар көбінесе графиттен жасалынады. Егер бір электролиттің ерітіндісі немесе балқымасына екі электродты салып тоқ көзін қосқанда электр шамы жануы қажет. Себебі электролиттерде электр тоғын иондар тасымалдайды. Ерітінділер мен балқымалардың ток өткізгіштігі осы иондардың концентрациясына тәуелді болады. Бейэлектролиттер олар ионға ыдырамай молекула күйін қалады сол себепті электр тоғын тасымалдау қабілеті болмайды. Егер заттар суда ерімесе онда олар молекула күйінде ( тұнба, газ) болады.
Электролиттік диссоциация
Электролиттер суда ерігенде олар ионға ыдырайды, олар оң зарядты – катионға және теріс зарядты – анионға.
NaCl = Na+ + Cl-
Қышқылдар – сутегі катиондарына және қышқыл қалдығының аниондарына диссоциацияланатын электролиттер:
НAn ↔ Н+ + An- H3PO4 = 3H+ + PO43-
Негіздер – металл катиондарына және гидроксид иондарға диссоциацияланатын электролиттер:
KtОН ↔ Kt+ + ОН- NaOH = Na+ + OH-
Тұздар – металл катиондарына және қышқыл қалдығының аниондарына диссоциацияланатын электролиттер:
KtAn ↔ Kt+ + An- K2SO4 = 2K+ + SO42-
Электролиттік диссоциация механизмі
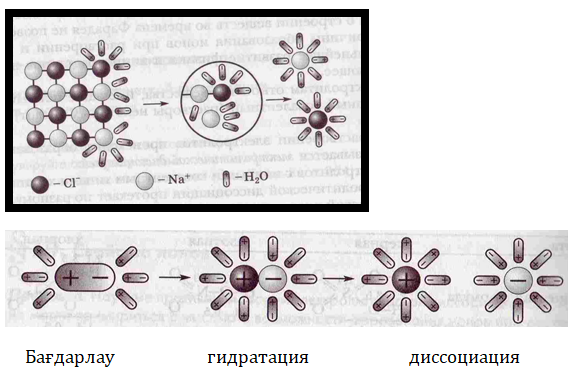
Иондық байланыс заттары: су дипольдерін бағдарлау → гидратация → диссоциация
NaCl ерітіндісінің диссоциациялануы
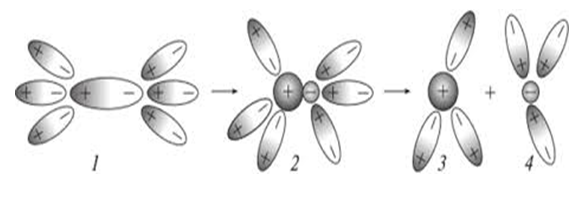
Ковалетті байланысы бар заттар: Ориентация → гидратациялануы → ионизация → диссоциация